Dlaczego głowy komet są zielone, ale ich ogony już nie? Zagadka dotycząca kolorów komet właśnie została rozwiązana, a licząca 90 lat teoria, która próbowała objaśniać to zjawisko – potwierdzona.
Co jakiś czas Pas Kuipera i Obłok Oorta rzucają w naszą stronę galaktyczne śnieżki złożone z lodu, pyłu i skał: pozostałości po powstaniu Układu Słonecznego sprzed 4,6 miliarda lat, które nazywamy kometami. W Układzie Słonecznym jest około 3700 znanych komet, chociaż podejrzewa się, że może ich być o miliardy więcej. Typowe jądro komety ma 10 kilometrów szerokości, ale jej koma jest często 1000 razy większa.
Komety przechodzą kolorową metamorfozę podczas swojej podróży ku Słońcu. W miarę zbliżania się do naszej gwiazdy, głowy wielu komet zyskują lśniąco zielony kolor, który staje się jaśniejszy, gdy komety zbliżają się do Słońca. Co dziwne jednak, ten zielony odcień utrzymuje się tylko na głowie komety i zanika, zanim dotrze do jednego lub dwóch warkoczy ciągnących się za kometą.
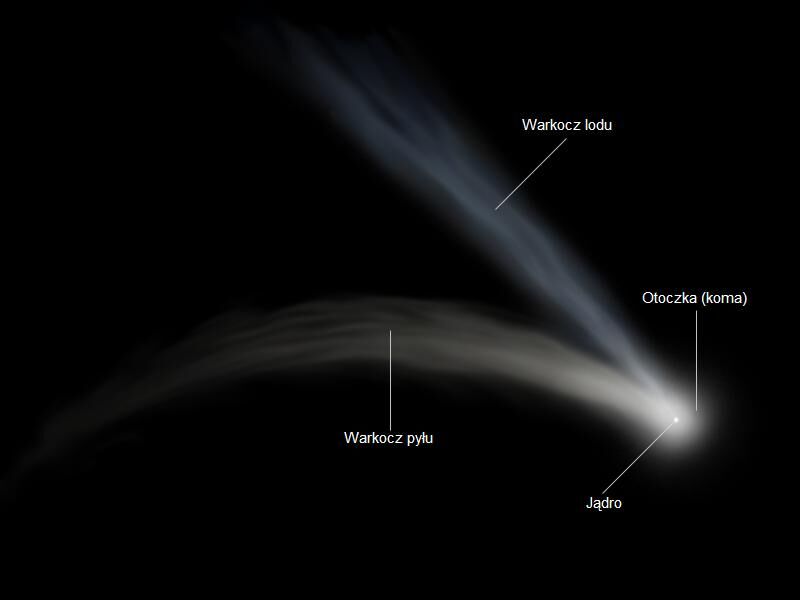
Na ilustracji: Schemat budowy komety. Źródło: Wikimedia Commons.
Jasne komety mogą organizować spektakularne pokazy dla tych, którzy mają szczęście je zobaczyć. W przeszłości jednak komety mogły zrobić coś więcej dla Ziemi. Jedna z teorii na temat pochodzenia życia głosi, że komety kiedyś dostarczyły cegiełki życia prosto pod nasze drzwi. Różne cząsteczki zawierające węgiel były dostarczane na powierzchnię naszej planety, gdzie wchodziły w kolejne złożone reakcje chemiczne, co mogło doprowadzić do powstania życia.
Astronomów, naukowców i chemików tajemnica kolorów komet intrygowała od prawie wieku. W latach 30. XX wieku fizyk Gerhard Herzberg wysnuł teorię, że zjawisko to jest spowodowane niszczeniem przez światło słoneczne dwuatomowego węgla (znanego również jako diwęgiel lub C2), związku chemicznego powstałego w wyniku interakcji między światłem słonecznym a materią organiczną na głowie komety. Niestety, ponieważ diwęgiel nie bardzo reaktywny i niestabilny, ta teoria była trudna do przetestowania.

Na zdjęciu: Gerhard Herzberg ur. 25 grudnia 1904 w Hamburgu, Niemcy, zm. 3 marca 1999 w Ottawie, Kanada, pionierski fizyk i fizykochemik, który w 1971 roku otrzymał Nagrodę Nobla w dziedzinie chemii „za wkład w poznanie struktury elektronowej i geometrii cząsteczek, zwłaszcza wolnych rodników". Źródło: Alchetron
Do zrozumienia właściwości diwęgla konieczne są podstawy mechaniki kwantowej, za pomocą której można modelować zachowanie i reakcje cząsteczek w różnych sytuacjach. W przyrodzie, do modelowego zachowania wkradają się jednak perturbacje, czyli odchylenia od modelu, które bywają tak duże, że spektroskopiści często rezygnują z analizy zebranych danych i określają obserwowane widma cząsteczki jako »silnie zaburzone«”. Sam Gerhard Herzberg, który był bliski stworzenia spektroskopii małych cząsteczek i który rozpoczął badania mające wyjaśnić dlaczego warkocze komet nigdy nie są zielone, zwykle odkładał badanie perturbacji na bok, tak by czekały „na lepsze czasy”.
Praca Herzberga znalazła kontytunację w badaniach Roberta W. Fielda pracującego w Massachusetts Institute of Technology (MIT), którego ciekawiło „niewłaściwe zachowanie” cząsteczek, a w szczególności tlenku węgla. Dalsze prace Fielda nad badaniem perturbacji stanu C cząsteczki C2 doprowadziły badaczy do odkrycia, że źródłem obserwowanych perturbacji w cząsteczce C2 jest nowe zjawisko dotyczące konfiguracji elektronów i dziur walencyjnych. Okazało się, że pomimo prostoty swojego składu chemicznego, diwęgiel posiada zaskakująco skomplikowaną strukturę elektronową, która wykazuje ostre anomalie poziomów energii. Oznaki „perturbacji spektroskopowych” diwęgla są znacznie liczniejsze i bardziej złożone niż te, które można znaleźć w innych prostych, opisywanych w podręcznikach molekułach dwuatomowych, takich jak CO, N2 i O2.
Zaburzenia spowodowane przez te nieoczekiwane i zaskakująco stabilne konfiguracje dziur walencyjnych mają duży wpływ na właściwości fotodysocjacyjne i predysocjacyjne C2, które określają, jak długo cząsteczki C2 przetrwają na komecie, zanim zostaną zniszczone przez promieniowanie ultrafioletowe światła słonecznego. Podsumowując, tajemniczo brzmiące określania perturbacja, predysocjacja i fotodysocjacja to trzy arkana spektroskopowe, które wyjaśniają tajemnicę różnicy kolorów między głową a ogonem uderzająco widocznej komety.
Te spostrzeżenia były kluczowe dla rozwiązania prawie stuletniej zagadki dotyczącej kolorów komet, którą badał profesor Timothy W. Schmidt z Uniwersytetu Nowej Południowej Walii (UNSW) w Australii. Połączenie wyników badań tych zespołów co doprowadziło do tego, że po raz pierwszy w historii naukowcy zaobserwowali szczegóły oddziaływania chemicznego, o którym teoretyzował Herzberg w latach 30. XX wieku, pokazując, że ta 90-letnia teoria jest poprawna.
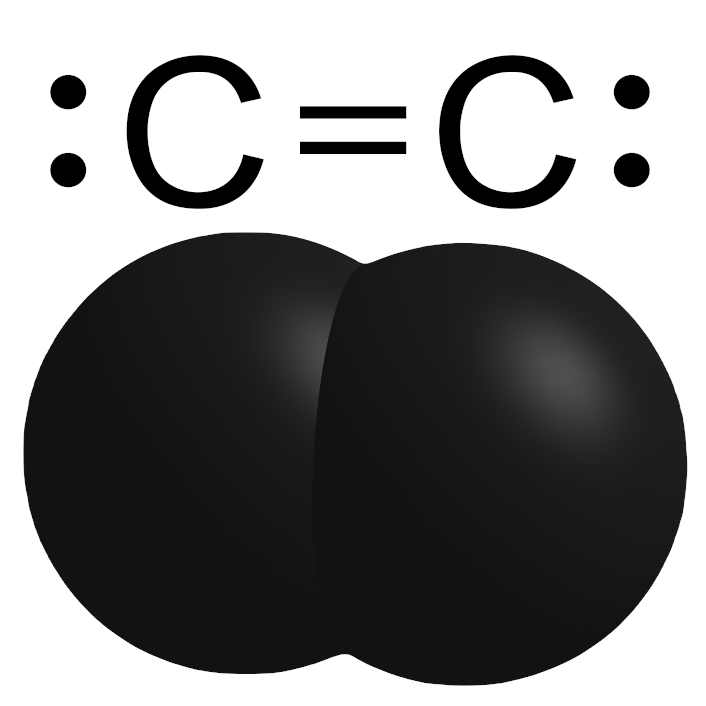
Na ilustracji: Struktura wiązania chemicznego i przestrzenny model cząsteczki diwęgla, C2. Źródło: Wikipedia
Kluczowy gracz znajdujący się w centrum tej tajemnicy, diwęgiel, składa się z dwóch atomów węgla i jest bardzo reaktywny. Można go znaleźć tylko w ekstremalnie energetycznych lub niskotlenowych środowiskach, takich jak gwiazdy, komety i ośrodek międzygwiazdowy. Co ciekawe, diwęgiel nie występuje na kometach, dopóki nie zbliżą się one do Słońca. Gdy Słońce zaczyna nagrzewać kometę, materia organiczna w lodowym jądrze odparowuje i przechodzi do komy. Światło słoneczne następnie rozbija większe cząsteczki organiczne, w rezultacie czego powstaje diwęgiel.
Gdy kometa zbliża się jeszcze bardziej do Słońca, promieniowanie UV rozbija molekuły diwęgla, które niedawno wytworzyła w procesie zwanym „fotodysocjacją”. Proces ten niszczy diwęgiel, zanim będzie mógł się on oddalić od jądra komety, powodując rozjaśnienie i kurczenie się zielonej komy oraz sprawiając, że zielony odcień nigdy nie przedostanie się do kometarnego ogona.

Na ilustracji: Kometa C/2014 Q2 Lovejoy nad Tucson w Arizonie w 2015 r. Źródło: John Vermette
Aby rozwiązać zagadkę koloru komet, zespół musiał odtworzyć pozaziemski proces chemiczny w kontrolowanym środowisku na Ziemi. Wykorzystano do tego komorę próżniową i wiele laserów. Najpierw jednak musiano stworzyć cząsteczkę, która jest zbyt reaktywna, aby przechowywać ją w butelce. Dokonano tego biorąc większą cząsteczkę, znaną jako perchloroetylen lub C2Cl4, i odstrzeliwując jej atomy chloru (Cl) za pomocą lasera UV o dużej mocy. Nowo powstałe cząsteczki diwęgla zostały następnie popchnięte przez wiązkę gazu do komory próżniowej o długości około dwóch metrów. Tam na diwęgiel zostały skierowane kolejne dwa lasery UV: jeden, który zalewał cząsteczki promieniowaniem, a drugi, który powodował, że powstające atomy węgla były wykrywalne. Uderzenie promieniowania rozrywało bowiem diwęgiel, kierując atomy węgla do detektora prędkości. Ze względu na złożoność eksperymentu, potrzeba było aż dziewięciu miesięcy by dokonać pierwszego pomiaru, jednak warto było czekać i dokładać starań. Była to pierwsza obserwacja tej reakcji chemicznej przeprowadzona w laboratorium na Ziemi.
Więcej informacji:
- Publikacja „Photodissociation of dicarbon: How nature breaks an unusual multiple bond” Jasmin Borsovszky i in. Proceeding of National Academy of Sciences (2021) 118 (52) e2113315118
Opracowanie: Joanna Molenda-Żakowicz
Na ilustracji: Wizja artystyczna komety w przestrzeni kosmicznej. Źródło: SciTechDaily